فهرست عناوین
- مقدمه
- اسید نیتریک : جزء کلیدی در تولید مواد منفجره قوی
- واکنش نیتراسیون : اسید نیتریک چگونه ترکیبات انفجاری ایجاد می کند
- تولید TNT (تری نیتروتولوئن) با اسید نیتریک
- نیتروگلیسیرین و اختراع دینامیت
- نیتروسلولز : پنبه انفجاری تولید شده از پنبه با استفاده از اسید نیتریک
- RDX و HMX : مواد منفجره از نوع نیترو آمین تولید شده با اسید نیتریک
- PETN و دیگر مواد منفجره از نوع نیترات استر
- مقایسه مواد منفجره اصلی تولید شده با اسید نیتریک
- تکنیک اسید مخلوط : استفاده از اسید سولفوریک همراه با اسید نیتریک
- تولید صنعتی اسید نیتریک برای ساخت مواد منفجره
نوشته شده توسط شرکت صنایع نیتریک ایران
منتشر شده توسط شرکت صنایع نیتریک ایران
تاریخ انتشار مقاله : 18-05-1404
تاریخ بروزرسانی مقاله : 18-05-1404
تعداد کلمات : 3000
آدرس مقاله : لینک مقاله
کاربرد نیتریک در ساخت مواد منفجره مانند tnt و دینامیت ها

مقدمه
اسید نیتریک (HNO3) یک اسید معدنی بسیار خورنده و قوی است که در تولید مواد منفجره نقش بسیار مهمی ایفا می کنند. این ماده یکی از مواد شیمیایی کلیدی به شمار می رود که برای ایجاد بسیاری از ترکیبات معروف انفجاری از جمله TNT تری نیتروتولوئن و دینامیت مورد استفاده قرار می گیرد. با افزودن گروه های نیترو (-NO2) به مولکول های آلی از طریق فرایندی به نام نیتراسیون (نیتره کردن) ، اسید نیتریک می تواند مواد پایدار را به موادی بسیار پرانرژی تبدیل کند. این توانایی در ایجاد ترکیبات نیترو باعث شده است اسید نیتریک چه در گذشته و چه در دوران مدرن یک جزء ضروری در تولید مواد منفجره باشد. در این بررسی جامع به نحوه کاربرد اسید نیتریک در ساخت انواع مواد منفجره ، فرایندهای شیمیایی مربوطه و جنبه های تاریخی ، صنعتی و ایمنی استفاده از آن در صنعت مواد منفجره می پردازیم.
اسید نیتریک : جزء کلیدی در تولید مواد منفجره قوی
بسیاری از مواد منفجره قوی که در کاربردهای نظامی و صنعتی به کار می روند با استفاده از خرید اسید نیتریک شیراز فله به عنوان یک جزء اساسی ساخته می شوند. اسید نیتریک به خودی خود یک ماده منفجره نیست ، اما گروه های نیترو لازم برای تبدیل مواد عادی به مواد انفجاری را فراهم می کند. وارد کردن این گروه های نیترو به مولکول ها ناپایداری و انرژی آن ها را به میزان زیادی افزایش می دهد و امکان احتراق یا انفجار سریع را فراهم می سازد. در حقیقت از اواسط قرن نوزدهم تاکنون اسید نیتریک مستقیماً مسئول ابداع اکثر مواد منفجره جدید بوده است و جایگزین مواد منفجره ضعیف تر قدیمی مانند باروت سیاه شده است. توانایی HNO3 به عنوان یک عامل نیتره کننده به این معنی است که می تواند موادی مانند تولوئن ، گلیسیرین یا سلولز را به مواد منفجره قدرتمند تبدیل کند. بدون اسید نیتریک تولید مواد منفجره معروفی مانند TNT، نیتروگلیسیرین و RDX در مقیاس وسیع امکان پذیر نبود.
واکنش نیتراسیون : اسید نیتریک چگونه ترکیبات انفجاری ایجاد می کند
فرایند شیمیایی اصلی که به وسیله آن اسید نیتریک به ایجاد ترکیبات انفجاری می پردازد ، نیتراسیون نامیده می شود. در واکنش نیتراسیون اسید نیتریک یک گروه نیترو (-NO2) را به مولکول آلی وارد می کند و معمولاً جایگزین یک اتم هیدروژن می شود. این دگرگونی خواص مولکول را کاملاً تغییر می دهد و اغلب یک ماده نسبتاً خنثی را به ماده ای بسیار پرانرژی و انفجاری تبدیل می کند. برای مثال زمانی که اسید نیتریک با ترکیبات آروماتیکی مانند تولوئن واکنش می دهد ، می تواند یک یا چند گروه نیترو را به حلقه بنزن اضافه کند و محصولاتی مانند مونو نیتروتولوئن ، دی نیتروتولوئن و در نهایت تری نیتروتولوئن (TNT) ایجاد کند. به همین ترتیب وقتی اسید نیتریک با الکل ها واکنش می کند (با کمک اسید سولفوریک به عنوان کاتالیزور)، استرهای نیتراتی ایجاد میشود؛ برای نمونه، گلیسیرین را به نیتروگلیسیرین و پنتا اریتریتول را به پنتا اریتریتول تترا نیترات (PETN) تبدیل می کند. در عمل برای انجام این واکنش ها نیاز به اسید نیتریک غلیظ (معمولاً بالای 90% یا حتی اسید نیتریک دودکننده 98%) است. نیتره کردن با اسید نیتریک خالص مقداری آب به عنوان محصول جانبی تولید می کند که می تواند واکنش را کند یا متوقف کند ؛ به همین دلیل معمولاً از مخلوطی از اسید نیتریک و اسید سولفوریک استفاده می شود. اسید سولفوریک آب تولید شده را جذب می کند و یون نیترو نیوم فعال را ایجاد می کند که به مولکول آلی حمله می کند. فرایند نیتراسیون نیاز به کنترل دقیق دما دارند ، زیرا این واکنش ها شدیداً گرمازا هستند و در صورت عدم مدیریت صحیح ممکن است از کنترل خارج شده و منجر به آتش سوزی یا انفجار شوند. با کنترل غلظت اسیدها ، دمای واکنش و مدت زمان آن ، شیمی دانان می توانند تعداد گروه های نیتروی دلخواه را وارد مولکول کنند که مستقیماً قدرت انفجاری ماده حاصل را تعیین می کند.
تولید TNT (تری نیتروتولوئن) با اسید نیتریک
TNT یا تری نیتروتولوئن 2,4,6 ، یکی از مشهورترین مواد منفجره است که مستقیماً از طریق نیتره کردن تولوئن توسط اسید نیتریک تولید می شود. تولید صنعتی TNT عموماً یک فرایند نیتره کردن سه مرحله ای است. در مرحله اول تولوئن را با مخلوطی از اسید نیتریک و اسید سولفوریک نیتره می کنند تا مونو نیتروتولوئن (MNT) تشکیل شود. MNT جدا شده و سپس با انجام نیتره کردن قوی تر به دی نیتروتولوئن (DNT) تبدیل می شود. در مرحله نهایی DNT با مخلوط بدون آب اسید نیتریک بسیار غلیظ و اولئوم (اسید سولفوریک دارای SO3 اضافی) نیتره می شود تا تری نیتروتولوئن (TNT) حاصل گردد. در تمام این مراحل اسید سولفوریک آب تشکیل شده را جذب می کند و به تولید یون نیترو نیوم کمک می کند ، در حالی که اسید نیتریک گروه های نیترو لازم در هر مرحله را فراهم می نماید. اسید نیتریک در هر مرحله واکنش مصرف می شود ، اما مقدار زیادی از اسید سولفوریک بعد از فرایند قابل بازیابی و استفاده مجدد است. پس از نیتره کردن و تولید TNT، معمولاً آن را با شستشو و تثبیت ، کریستالیزه یا پالایش می کنند تا ایزومرهای ناپایدار و سایر محصولات جانبی نامطلوب حذف شوند. محصول نهایی یک جامد بلوری زرد رنگ است که نسبت به شوک و حرارت در مقایسه با بسیاری از مواد منفجره پرقدرت دیگر نسبتاً پایدار است. پایداری و سهولت استفاده از TNT (نقطه ذوب حدود 80 درجه سانتی گراد که اجازه می دهد به راحتی ذوب شده و درون پوسته های مهمات ریخته شود) باعث شد که در اوایل قرن بیستم به ماده منفجره نظامی اصلی تبدیل شود. استفاده از اسید نیتریک در این فرایند چند مرحله ای تحت کنترل دقیق ، امکان تولید مؤثر TNT را در مقیاس صنعتی فراهم می سازد.
نیتروگلیسیرین و اختراع دینامیت
نیتروگلیسیرین یک ماده منفجره مایع و بسیار قوی است که از نیتره کردن گلیسیرین با مخلوطی از اسید نیتریک و اسید سولفوریک ساخته می شود. این فرایند نخستین بار در سال 1847 توسط شیمیدان ایتالیایی آسکانیو سوبرو کشف شد که ویژگی های انفجاری شدید این ماده را مشاهده کرد. نیتروگلیسیرین (با فرمول شیمیایی C3H5N3O9) از نظر فنی یک نیترات استر است. در اصل همان گلیسیرینی است که سه گروه هیدروکسیل (–OH) آن توسط اسید نیتریک به گروههای نیترات (–ONO2) تبدیل شده اند. این ماده در عین حال که فوق العاده قوی است ، در حالت خالص خود به شدت به ضربه حساس است و کار کردن با آن بسیار خطرناک است. در سال های اولیه کار با این ماده ، به دلیل تمایل آن به انفجار بر اثر کوچک ترین تکان یا تغییر دما سوانح فاجعه باری رخ داد. پیشرفت بزرگی در ایمن تر کردن استفاده از نیتروگلیسیرین در دهه 1860 توسط آلفرد نوبل حاصل شد. نوبل دریافت که با مخلوط کردن نیتروگلیسیرین مایع با یک ماده جاذب خنثی (زمین دیاتومه که با نام کیزلگور نیز شناخته می شود) می توان آن را به صورت خمیر پایدارتر درآورد. او در سال 1867 این مخلوط را با نام دینامیت به ثبت رساند و آن را به عنوان یک ماده منفجره ایمن برای کاربردهای معدن کاوی و ساختمانی معرفی کرد. دینامیت این امکان را داد که قدرت عظیم نیتروگلیسیرین با ریسک بسیار کمتر انفجار تصادفی در هنگام حمل و نقل یا کار با آن مهار شود. اسید نیتریک برای تولید نیتروگلیسیرین درون دینامیت ضروری بود و نشان داد که توانایی نیتره کردن این اسید به طور مستقیم به یکی از مهم ترین اختراعات در تاریخ مواد منفجره منجر شد. دینامیت به سرعت جایگزین مواد منفجره کم قدرت تر در پروژه های مهندسی شد و نام آلفرد نوبل در سراسر جهان مشهور ساخت.
نیتروسلولز : پنبه انفجاری تولید شده از پنبه با استفاده از اسید نیتریک
نیتروسلولز که با نام پنبه انفجاری (گان کاتن) نیز شناخته می شود ، ماده ای انفجاری است که از اشباع کردن پنبه یا سایر الیاف سلولزی در اسید نیتریک (معمولاً در حضور اسید سولفوریک) به دست می آید. در این فرایند نیتره کردن گروه های هیدروکسیل موجود در پلیمر سلولز با گروه های نیترات جایگزین می شوند و حاصل آن نیترات سلولز است. کشف نیتروسلولز در سال 1846 توسط کریستیان فریدریش شون بین یک نقطه عطف مهم بود ، زیرا یکی از نخستین مواد منفجره قوی بود که با شیمی اسید نیتریک ساخته شد. کاربرد اسید نیتریک در صنایع رنگ و رنگدانه ها نیز گسترده است و به تولید انواع رنگهای آلی و معدنی کمک می کند. پنبه انفجاری این نام را گرفت زیرا الیاف پنبه که در مخلوط اسیدها غوطه ور می شدند پس از خشک شدن به صورت کرک سفیدرنگی درمی آمدند که بسیار سریع تر از پنبه معمولی می سوزد یا منفجر می شود. وقتی نیتروسلولز به درجه بالایی نیتره شود می تواند تقریباً به صورت آنی بسوزد و حجم بزرگی از گازهای داغ تولید کند. ویژگی ای که آن را به عنوان پیشرانه در سلاح های گرم و توپخانه (به شکل باروت بی دود) مفید می سازد. بر خلاف باروت سیاه ، پیشرانه های مبتنی بر نیتروسلولز بدون تولید دود غلیظ می سوزند که این یک مزیت مهم در جنگ ها بود. با این حال ساخت نیتروسلولز در ابتدا با ایمنی پایین همراه بود ؛ اگر هرگونه اسید باقی مانده در ماده می ماند ممکن بود به طور خودبه خود مشتعل شود یا به مرور زمان تجزیه گردد. در طول سال ها روش های تولید با شستشوی کامل و پایدارسازی الیاف نیتره شده بهبود یافت. بدین ترتیب اسید نیتریک امکان ساخت پیشرانه ها و مواد انفجاری مبتنی بر نیتروسلولز را فراهم کرد که پیشرفت عظیمی در فناوری مهمات در قرن نوزدهم محسوب می شد.
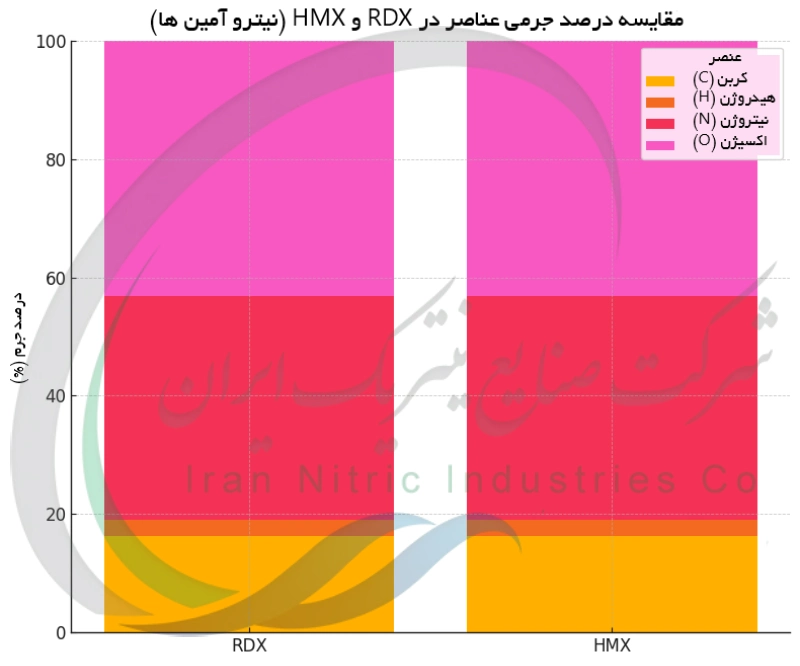
RDX و HMX : مواد منفجره از نوع نیترو آمین تولید شده با اسید نیتریک
RDX (سیکلو تری متیلن تری نیترو آمین معروف به هگزوجن یا سیکلونیت) یک ماده منفجره بسیار قوی است که وجود خود را مدیون شیمی مبتنی بر اسید نیتریک است. RDX متعلق به دسته ای از مواد منفجره به نام نیترو آمین ها است که در مولکول آن ها گروه های نیترو به اتم های نیتروژن متصل شده اند. این ماده نخستین بار حوالی سال 1898 توسط شیمیدان آلمانی جورج فردریش هنینگ سنتز شد ؛ او RDX را از واکنش هگزا متیلن تترامین (هگزامین) با اسید نیتریک دودکننده به دست آورد. RDX به طور قابل توجهی از TNT قوی تر است ، اما برای سال ها به دلیل سختی تولید انبوه به صورت گسترده به کار گرفته نشد. تا زمان جنگ جهانی دوم روش های تولید کارآمد (مانند فرایند باخمن که در آن از اسید نیتریک و نیترات آمونیوم در یک مخلوط واکنش استفاده می شود) توسعه نیافتند که امکان ساخت RDX را در مقیاس صنعتی فراهم کنند. در طی جنگ جهانی دوم ، RDX به یک جزء کلیدی در مواد منفجره نظامی تبدیل شد و اغلب آن را با TNT یا عوامل دیگر مخلوط می کردند. برای مثال در ترکیباتی مانند Torpex و ترکیب B .
HMX (سیکلو ترامتیلن تترا نیترامین) ماده منفجره هم خانواده RDX است که به عنوان محصول فرعی تولید RDX کشف شد و بعدها برای کاربردهای ویژه بهینه سازی گردید. HMX سرعت انفجار و پایداری حتی بالاتری نسبت به RDX دارد. مانند RDX ، این ماده نیز از نیتره کردن هگزامین یا پیش سازهای مشابه تحت شرایط بسیار قوی با اسید نیتریک تولید می شود. هر دوی این مواد نشان می دهند که چگونه اسید نیتریک امکان خلق مولکول های انفجاری پیشرفته ای را فراهم می کند که قدرت انفجاری بسیار زیادی دارند. امروزه RDX همچنان به طور گسترده استفاده می شود به ویژه به عنوان جزء اصلی ماده انفجاری پلاستیکی C4 و HMX در کاربردهایی به کار می رود که نیاز به قدرت یا پایداری حتی بیشتر است (مانند برخی چاشنی های انفجاری تسلیحات هسته ای و پیشرانه های راکتی).
PETN و دیگر مواد منفجره از نوع نیترات استر
پنتا اریتریتول تترا نیترات (PETN) یکی دیگر از مواد منفجره پرقدرت است که با استفاده از اسید نیتریک سنتز می شود. PETN یک نیترات استر است ، مشابه نیتروگلیسیرین ، اما به صورت یک جامد بلوری سفید وجود دارد. این ماده از نیتره کردن پنتا اریتریتول با اسید نیتریک غلیظ به دست می آید و معمولاً واکنش در دماهای پایین کنترل می شود. PETN نخستین بار در سال 1894 در آلمان تهیه شد و در طول قرن بیستم به خاطر قدرت انفجاری بالا بریسانس و سرعت انفجار بیش از TNT) و پایداری نسبی اش مور توجه قرار گرفت. PETN به خاطر کاربردش در طناب انفجاری (پرایماکورد) مشهور است ، جایی که هسته ای از PETN موج انفجار را به سرعت در طول خود منتقل می کند. همچنین به عنوان خرج تقویتی در کلاهک ها و در برخی ترکیبات انفجاری پلاستیکی استفاده می شود. به عنوان یک ماده منفجره از نوع نیترات استر ، تولید PETN نیازمند اسید نیتریک به عنوان عامل نیتره کننده است تا چهار گروه نیترو به مولکول پنتا اریتریتول متصل شوند. نتیجه آن مولکولی است که از نظر داشتن اتم های اکسیژن و نیتروژن بسیار غنی است و قابلیت تجزیه بسیار سریعی دارد. علاوه بر PETN ، نیترات استرهای دیگری نیز با شیمی مشابه تولید شده اند : برای نمونه اتیلن گلیکول دی نیترات (EGDN) از نیتره کردن اتیلن گلیکول به دست می آید و گاهی همراه با نیتروگلیسیرین در برخی دینامیت ها برای مقاومت بیشتر در برابر انجماد به کار می رفت. مواد منفجره نوع نیترات استر معمولاً بسیار قوی هستند اما نسبت به ضربه و اصطکاک حساسیت دارند و باید با دقت فرمول بندی و جابجا شوند. توسعه PETN و ترکیبات مرتبط نشان دهنده انعطاف پذیری بالای کاربرد اسید نیتریک در خلق طیفی از مواد منفجره با خواص گوناگون برای کاربردهای تخصصی است.
مقایسه مواد منفجره اصلی تولید شده با اسید نیتریک
اسید نیتریک برای تولید انواع گسترده ای از مواد منفجره به کار رفته است که هر کدام ویژگی ها و کاربردهای منحصر به فردی دارند. برخی از مواد منفجره مبتنی بر اسید نیتریک نسبتاً پایدار هستند و برای استفاده در مهمات مناسب اند مثلاً TNT برای خرج گلوله های توپ به دلیل پایداری اش ترجیح داده می شود در حالی که برخی دیگر بسیار حساس یا بسیار قوی اند و فقط در نقش های خاصی به کار می روند (برای نمونه نیتروگلیسیرین با اینکه قدرت زیادی دارد ، به دلیل ناپایداری زیاد به تنهایی استفاده نمی شود و عمدتاً در دینامیت یا ترکیبات پیشران به کار می رود). از نظر ماهیت شیمیایی نیز این مواد تفاوت هایی دارند : برخی ترکیبات نیتروآروماتیک هستند (مانند TNT و اسید پیکریک که در آن ها گروه های نیترو به حلقه های آروماتیک متصل شده اند ؛ برخی دیگر استرهای نیتراته هستند مانند نیتروگلیسیرین PETN و نیتروسلولز که از واکنش اسید نیتریک با گروه های الکلی حاصل می شوند و گروهی نیز نیتروآمین مانند RDX و HMX هستند که در آن ها اسید نیتریک گروه های نیترو را به ساختارهای آمینی اضافه می کند. افزون بر این اسید نیتریک در تولید مواد منفجره معدنی مانند نیترات آمونیوم نیز نقش دارد. ترکیبی که خود یک ماده آلی نیتردار نیست اما یک اکسیدکننده حیاتی در بسیاری از مواد منفجره به شمار می آید. برای نشان دادن تفاوت ها و شباهت های بین برخی از مهم ترین مواد منفجره حاصل از شیمی اسید نیتریک ، جدول زیر اطلاعات کلیدی را درباره تعدادی از آن ها خلاصه می کند. در این مقایسه فرمول شیمیایی ، ماده اولیه ای که نیتره می شود (پیش ساز) ، نوع یا رده ترکیب انفجاری و کاربردهای معمول هر کدام ذکر شده است:
| ماده منفجره | فرمول شیمیایی | ماده اولیه | نوع ترکیب | کاربردهای اصلی |
|---|---|---|---|---|
| TNT (تری نیتروتولوئن) | C7H5N3O6 | تولوئن | ترکیب نیتروآروماتیک (ترینیتروتولوئن) | خرج نظامی در گلولهها و بمبها، تخریب سازهها |
| نیتروگلیسیرین | C3H5N3O9 | گلیسیرین | نیترات استر (ترینیترات) | استفاده در دینامیت (برای انفجار)، همچنین در برخی پیشرانها و به مقدار کم به عنوان دارو |
| نیتروسلولز (پنبه انفجاری) | (C6H7(NO2)3O5)n | سلولز (پنبه) | نیترات استر (پلیمر) | پیشرانه در مهمات (باروت بیدود)، خرج انفجاری پنبهای، فیلمهای اولیه عکاسی |
| RDX | C3H6N6O6 | هگزامین (هگزامتیلنتترامین) | نیتروآمین | ماده منفجره نظامی پرقدرت (مثلاً در C4 پلاستیکی، اژدرها، خرجهای تقویتی) |
| PETN | C5H8N4O12 | پنتااریتریتول | نیترات استر (تترانیترات) | طناب انفجاری (پرایماکورد)، خرجهای تقویتی، برخی مواد پلاستیکی انفجاری، چاشنیها |
| اسید پیکریک | C6H3N3O7 | فنول (کربولیک اسید) | ترکیب نیتروآروماتیک (ترینیتروفنول) | خرج انفجاری در گلولهها (به صورت تاریخی مِلینیت یا لیدیت؛ امروزه به دلیل ناپایداری تقریباً کنار گذاشته شده) |
| نیترات آمونیوم | NH4NO3 | آمونیاک + اسید نیتریک (واکنش خنثیسازی) | اکسیدکننده معدنی | ماده منفجره صنعتی (مخلوط ANFO در معادن)، کود شیمیایی (در شرایط خاص یا با افزودن سوخت قابل انفجار است) |
تکنیک اسید مخلوط : استفاده از اسید سولفوریک همراه با اسید نیتریک
در تولید بسیاری از مواد منفجره بر پایه اسید نیتریک به جای استفاده از اسید نیتریک خالص از اسید مخلوط (ترکیب اسید نیتریک و اسید سولفوریک) بهره می برند. دلیل اصلی این انتخاب به واکنش نیتراسیون باز می گردد ؛ هنگام افزودن گروه نیترو به یک مولکول آلی ، آب به عنوان محصول جانبی تشکیل می شود که غلظت اسید نیتریک را کاهش داده و می تواند واکنش را متوقف کند. اسید سولفوریک به عنوان عامل آب گیر قوی ، این آب را جذب کرده و علاوه بر آن با پروتون دهی به اسید نیتریک یون فعال نیترو نیوم (NO₂⁺) را برای نیتراسیون فراهم می کند. این روش در تولید TNT، نیتروگلیسیرین ، نیتروسلولز و اسید پیکریک به کار میرود. در فرایندهایی مانند تولید نیتروگلیسیرین ، گلیسیرین به آرامی به مخلوط سرد HNO₃ و H₂SO₄ اضافه می شود تا واکنش تحت کنترل بماند. در موارد خاص از اولئوم استفاده می شود تا محیط کاملاً بدون آب باشد و امکان افزودن چندین گروه نیترو فراهم شود. پس از نیتراسیون ، اسیدها بازیابی و مجدداً استفاده می شوند تا هزینه و پسماند کاهش یابد. کارخانه های مدرن برای ایمنی ، از حسگرهای دما ، سیستم های خنک کننده ، تجهیزات مقاوم به خوردگی و طراحی های ضدانفجار استفاده می کنند. با وجود این تدابیر کار با اسید مخلوط همچنان نیازمند دقت و کنترل بالا در صنعت مواد منفجره است.
تولید صنعتی اسید نیتریک برای ساخت مواد منفجره
دسترسی به مقادیر زیاد اسید نیتریک نقش مهمی در گسترش صنعت مواد منفجره داشته است. در قرن نوزدهم این اسید به صورت محدود و دسته ای از حرارت دادن نیترات های معدنی با اسید سولفوریک به دست می آمد که وابسته به منابع طبیعی نیترات بود. تحول بزرگ در اوایل قرن بیستم با توسعه فرآیند استوالد رخ داد که تولید انبوه اسید نیتریک از آمونیاک را ممکن ساخت. در این روش آمونیاک حاصل از فرآیند هابر-بوش اکسید شده و به اکسیدهای نیتروژن تبدیل می شود و سپس در آب حل شده تا اسید نیتریک تولید شود. این پیشرفت خصوصاً در جنگ جهانی اول به کشورها توان خودکفایی در تولید مواد منفجره داد. امروزه سالانه میلیون ها تن HNO₃ تولید می شود که بخش عمده آن برای کودهای شیمیایی و بخشی نیز برای ساخت مواد منفجره مانند TNT و RDX مصرف می گردد. برای نیتراسیون معمولاً اسید نیتریک غلیظ (۹۰–۱۰۰٪) یا اسید نیتریک دودکننده استفاده می شود که از طریق تقطیر یا افزودن اسید سولفوریک به دست می آید. بسیاری از کارخانه های مهمات سازی دارای واحد تغلیظ و بازیافت اسید هستند. این پیوند میان تولید اسید نیتریک و ساخت مواد منفجره ، زنجیره ای یکپارچه ایجاد کرد که صنعت و جنگ قرن بیستم را متحول ساخت.




