فهرست عناوین
- مقدمه
- آشنایی با اسید نیتریک
- نگاهی کلی به فرآیند تولید باتری های مدرن
- نقش اسید نیتریک در سنتز مواد کاتد
- نقش اسید نیتریک در آماده سازی مواد آند
- اسید نیتریک برای گرافن و نانومواد کربنی در باتری ها
- اسید نیتریک در الکترولیت ها و افزودنی های باتری
- مقایسه اسید نیتریک با سایر اسیدها در تولید باتری
- مزایای استفاده از اسید نیتریک در تولید باتری
- اقدامات ایمنی برای کار با اسید نیتریک
- نوآوری ها و پژوهش های جدید درباره اسید نیتریک در باتری ها
نوشته شده توسط شرکت صنایع نیتریک ایران
منتشر شده توسط شرکت صنایع نیتریک ایران
تاریخ انتشار مقاله : 22-05-1404
تاریخ بروزرسانی مقاله : 22-05-1404
تعداد کلمات : 2900
آدرس مقاله : لینک مقاله
نقش اسید نیتریک در تولید باتری های جدید

مقدمه
فناوری باتری های مدرن با سرعت زیادی پیشرفت کرده و منجر به ظهور باتری های لیتیوم-یون با کارایی بالا ، باتری های لیتیوم-سولفور و دیگر باتری های نسل جدید شده است. این باتری ها به مواد بسیار خالص و فرآیندهای ساخت دقیقی نیاز دارند. مواد شیمیایی گوناگونی در ساخت اجزای باتری به کار گرفته می شوند و اسید نیتریک یک عامل کلیدی در این میان به شمار می رود. اسید نیتریک در مراحل متعددی از تولید باتری نقش عمیقی ایفا می کند ، از آماده سازی مواد الکترود گرفته تا بازیافت سلول های کهنه. فرآیند تولید باتری های جدید مراحل زیادی دارند و اسید نیتریک در چندین مورد از آنها نقشی حیاتی ایفا می کند.
آشنایی با اسید نیتریک
اسید نیتریک (HNO₃) یک اسید معدنی قوی است که به خاطر ویژگی اکسیدکنندگی شدیدش شناخته می شود. در صنعت به طور گسترده برای تولید کودهای شیمیایی ، مواد منفجره و در بسیاری از سنتزهای شیمیایی به کار می رود. در زمینه ساخت باتری توانایی اسید نیتریک در حل کردن فلزات و تشکیل نمک های نیترات به آن ارزشی ویژه می بخشد. این اسید می تواند ترکیبات فلزی گوناگون را تجزیه کرده و محلول های با خلوص بالا ایجاد کند که بعدها برای ساخت الکترودها و الکترولیت های باتری مورد استفاده قرار می گیرند. ماهیت اکسیدکنندگی آن همچنین باعث می شود که بتواند سطوح مواد را اصلاح کند ، که این خود گامی مهم در آماده سازی اجزای پیشرفته باتری است.
نگاهی کلی به فرآیند تولید باتری های مدرن
تولید باتری های مدرن شامل مراحل و مواد متعددی است. تولیدکنندگان کار را با مواد اولیه ای مانند فلزات ، کربن ، مواد اتصال دهنده و الکترولیت ها آغاز می کنند و سپس آنها را درون سلول های باتری مونتاژ می کنند. بسیاری از این مراحل متکی به عملیات شیمیایی هستند تا اطمینان حاصل شود که مواد با استانداردهای سختگیرانه کیفیت مطابقت دارند. به عنوان مثال سنگ معدن ها و پودرهای خام اغلب نیاز به تصفیه دارند تا ناخالصی هایی که ممکن است به عملکرد باتری آسیب بزنند حذف شوند. محلول ها و اسیدهای شیمیایی برای شستشو ، اچ کردن یا پوشش دادن مواد به کار می روند. کاربرد اسید نیتریک در صنعت هوا و فضا نیز بسیار گسترده است و از آن برای فرآیندهایی مانند تمیزکاری آلیاژهای خاص ، آماده سازی سطوح و تولید قطعات دقیق استفاده می شود. اسید نیتریک در سراسر این فرآیندها کاربردهای متنوعی دارد. از سنتز مواد فعال گرفته تا تمیزکاری قطعات باتری ، این اسید به دستیابی به خلوص و کارایی بالای مورد نیاز در فناوری های جدید باتری کمک می کند.
نقش اسید نیتریک در سنتز مواد کاتد
یکی از کاربردهای حیاتی اسید نیتریک در سنتز مواد کاتد برای باتری های لیتیوم-یون و سایر باتری ها است. پودرهای کاتد مانند اکسیدهای لیتیم-نیکل-منگنز-کبالت یا فسفات آهن لیتیم (LFP) معمولاً از طریق واکنش های شیمیایی تولید می شوند که در آنها باید منابع فلزی حل شوند. اسید نیتریک اغلب برای انحلال و استخراج فلزاتی مانند نیکل ، کبالت و منگنز از اکسیدها یا ضایعات آنها استفاده می شود و محلولی از نیترات های فلزی به دست می دهد. این محلول های نیتراتی را می توان به طور همزمان به صورت هیدروکسیدها یا کربنات ها رسوب داد و سپس با تکلیس کردن آنها ، اکسید نهایی کاتد را تشکیل داد. استفاده از اسید نیتریک در این فرآیند بازده بالایی در انحلال فلزات دارد و نیترات هایی تولید می کند که به راحتی به ترکیبات مورد نظر تبدیل می شوند. علاوه بر این مسیر نیتراتی می تواند از ایجاد ناخالصی های ناخواسته جلوگیری کند ، برخلاف فرآیندهای مبتنی بر سولفات ، هیچ پسماند سولفاتی بر جا نمی گذارد که ممکن است کاتد را آلوده کند. در نتیجه ماده کاتد با خلوص بالا و کیفیت یکنواخت حاصل می شود که این امر به عملکرد بهتر باتری منجر می شود.
نقش اسید نیتریک در آماده سازی مواد آند
اسید نیتریک در آماده سازی مواد آند نیز نقش دارد به ویژه در آندهای پایه کربن مانند گرافیت. گرافیت طبیعی باید تا درجه خلوص مخصوص باتری (اغلب بالای ۹۹٪ کربن) تصفیه شود تا فلزات ردی یا سیلیکاهای جزئی در عمر باتری اختلال ایجاد نکنند. تیمارهای اسیدی از جمله شستشو با اسید نیتریک معمولاً برای حل کردن این ناخالصی ها از گرافیت استفاده می شوند. خرید اسید نیتریک کارون مخزن 1000 لیتری به طور موثری آلاینده های فلزی را از بین می برد و مواد آلی باقی مانده در گرافیت را اکسید می کند و خلوص آن را بهبود می بخشد بدون اینکه ساختار گرافیت تخریب شود. علاوه بر این اکسیداسیون کنترل شده با اسید نیتریک می تواند گروه های عاملی حاوی اکسیژن را بر سطح گرافیت ایجاد کند. این گروه ها ترشوندگی گرافیت را افزایش می دهند و کمک می کنند الکترولیت باتری به صورت یکنواخت تری در آند نفوذ کند و احتمالاً تشکیل یک لایه بین سطحی جامد پایدار (SEI) را بهبود می بخشند. در آندهای مبتنی بر سیلیکون که به تازگی توسعه یافته اند ، گاهی از مخلوط اسید نیتریک با سایر اسیدها برای اچ کردن سطوح سیلیکونی یا ایجاد ساختارهای نانومتخلخل استفاده می شود که این کار می تواند تنش حاصل از انبساط سیلیکون را کاهش دهد.
اسید نیتریک برای گرافن و نانومواد کربنی در باتری ها
باتری های پیشرفته اغلب از نانومواد کربنی مانند گرافن و نانولوله های کربنی برای بهبود رسانایی و ظرفیت استفاده می کنند. اسید نیتریک در فرآوری این مواد نقش اساسی دارد. در تولید اکسید گرافن (که پیش ماده گرافن است) ، از مخلوط اسید نیتریک و دیگر اسیدهای قوی برای اکسید کردن پودر گرافیت استفاده می شود. این فرآیند اکسیداسیون باعث نفوذ اسید بین لایه های گرافیت می شود و گروه های عاملی اکسیژنی را در آن وارد می کند و در نهایت گرافیت را به صورت لایههای اکسید گرافن جدا می سازد. سپس اکسید گرافن می تواند کاهش یابد تا گرافن رسانا حاصل شود و در بهبود عملکرد الکترودهای باتری به کار رود. به طور مشابه برای نانولوله های کربنی (CNT)، تیمارهای اسید نیتریک به طور گسترده ای برای عامل دار کردن سطوح آنها استفاده می شود. جوشاندن یا رفلاکس کردن نانولوله ها در اسید نیتریک ، گروه های کربوکسیل و سایر گروه های اکسیژن دار را به سطح این لوله ها اضافه می کند. این عامل دار شدن پراکندگی نانولوله ها را در دوغاب الکترود به میزان زیادی بهبود می بخشد و به پیوند خوردن آنها با مواد فعال و بایندرها کمک می کند. در نتیجه نانولوله های تیمار شده با اسید مسیرهای رسانایی بهتری را در الکترود فراهم می کنند و می توانند توان خروجی و پایداری باتری را افزایش دهند. حتی کربن فعال مورد استفاده در ابرخازن ها یا ابرخازن-باتری های هیبرید نیز گاهی با اسید نیتریک تیمار می شود تا نقص های سطحی و گروه های عاملی در آن ایجاد گردد که می تواند ظرفیت آن را افزایش دهد. بنابراین فرآوری نانومواد کربنی با اسید نیتریک یک گام کلیدی برای ادغام این مواد پیشرفته در سلول های باتری به شمار می رود.
اسید نیتریک در الکترولیت ها و افزودنی های باتری
اگرچه اسید نیتریک به طور مستقیم به عنوان الکترولیت باتری استفاده نمی شود ، اما در تولید ترکیبات کلیدی الکترولیت نقش مهمی دارد. نمونه بارز آن نیترات لیتیم (LiNO₃) است که در باتری های لیتیوم-سولفور به کار می رود و با تشکیل لایه محافظ روی آند لیتیمی ، واکنش های ناخواسته را کاهش داده و اثر شاتل پلیسولفیدها را مهار میکند ، در نتیجه عمر باتری بهبود می یابد. LiNO₃ از واکنش کربنات یا هیدروکسید لیتیم با اسید نیتریک تولید می شود. در باتری های آبی نوین نیز الکترولیت های مبتنی بر نیترات مانند نیترات روی مورد بررسی هستند که می توانند خواص الکتروشیمیایی ویژه ای ارائه دهند و نسبت به الکترولیت های سولفاته ، آسیب کمتری به الکترودها وارد کنند. علاوه بر این اسید نیتریک در تولید انواع نیترات های فلزی مورد استفاده برای پیش ماده های الکترولیت های جامد یا افزودنی ها نقش دارد. به طور کلی شیمی اسید نیتریک پشت صحنه بسیاری از نوآوریهای الکترولیتی است ، حتی اگر خود آن مستقیماً به عنوان الکترولیت اصلی به کار نرود.کاربرد اسید نیتریک در بازیافت باتری و بازیابی فلزات اسید نیتریک نقش مهمی در تولید و به ویژه بازیافت باتری های لیتیوم-یون ایفا می کند. در بازیافت این اسید بهعنوان عامل لیچینگ قدرتمند ، فلزاتی مانند لیتیم ، کبالت ، نیکل و منگنز را حتی از ترکیبات پایداری چون LiCoO₂ استخراج می کند. واکنش با پودر کاتد ، نیترات های محلول فلزی ایجاد می کند که به سرعت و با بازده بالا وارد محلول می شوند. یکی از مزیت های کلیدی این روش آن است که محلول نیترات به دست آمده می تواند بدون آلودگی اضافی مستقیماً در سنتز مواد کاتد جدید استفاده شود. اسید نیتریک علاوه بر فلزات کاتدی ، با حلکردن فویل مسی کلکتور و تبدیل آن به نیترات مس ، امکان بازیابی مس را فراهم می آورد. همچنین گرافیت باقیمانده آندها با ترکیب اسید نیتریک و حلال های دیگر تمیز شده و برای استفاده مجدد آماده می شود. این فرآیند چرخه عمر باتری را کامل می کند و مواد بازیافتی را به ترکیبات با خلوص بالا تبدیل کرده و دوباره به تولید باتری بازمی گرداند که این امر باعث حفظ منابع طبیعی و کاهش ضایعات صنعتی می شود.
مقایسه اسید نیتریک با سایر اسیدها در تولید باتری
در این زمینه مفید است که اسید نیتریک را با سایر اسیدهای متداول نظیر اسید سولفوریک ، اسید هیدروکلریک و اسیدهای آلی مقایسه کنیم. اسید سولفوریک (H₂SO₄) نیز اسید قوی دیگری است که به طور گسترده در صنعت به کار می رود به عنوان مثال در الکترولیت باتری های سرب-اسید و برخی روش های بازیافت. اسید کلریدریک (HCl) یک اسید قوی و عامل کاهنده است که برای تمیزکاری فلزات و برخی فرآیندهای لیچینگ استفاده می شود. اسیدهای آلی مانند اسید سیتریک نیز به عنوان جایگزین های سازگارتر با محیط زیست برای بازیافت باتری آزموده شده اند. هر یک از این اسیدها از نظر قدرت ، قابلیت اکسیداسیون ، نوع محصولات جانبی تولید شده و مشخصات ایمنی با دیگران تفاوت دارند. جدول زیر تفاوت ها و نقش های کلیدی اسید نیتریک را در مقایسه با این اسیدهای دیگر در فرآیندهای تولید باتری نشان می دهد.
| نوع اسید | قدرت اکسیداسیون | پسماند/محصولات جانبی | مزایا در فرآیند باتری | چالش ها / معایب |
|---|---|---|---|---|
| اسید نیتریک (HNO₃) | اکسیدکننده بسیار قوی؛ قادر به حل بسیاری از فلزات و اکسید کردن ترکیبات آلی. | نیترات های محلول تولید می کند؛ انتشار گازهای NOx (که می توان آنها را مهار یا بازیافت کرد). | برای حل کردن فلزات کاتدی و خالصسازی مواد بسیار مناسب؛ بدون پسماند جامد و دستیابی به محصول با خلوص بالا. | خورنده با دودهای سمی (NO₂)؛ نیازمند احتیاط زیاد در کار کردن و تصفیه گازهای NOx. |
| اسید سولفوریک (H₂SO₄) | اسید قوی ولی اکسیدکننده ضعیف تر (برای اکسید کردن نیاز به افزودنی دارد)؛ بدون عامل کاهنده روی برخی فلزات چندان موثر نیست. | سولفات های فلزی تولید می کند؛ می تواند ضایعات جامد ایجاد کند (مثلاً محصولات فرعی مانند گچ یا سولفات سدیم). | ارزان و بهوفور در دسترس؛ در باتری های سرب-اسید و برخی فرآیندهای لیچینگ به کار می رود. | پسماندهای سولفات می توانند محصولات را آلوده کنند؛ دفع ضایعات جامد مورد نیاز است؛ به تنهایی برای استخراج برخی فلزات به اندازه کافی موثر نیست. |
| اسید کلریدریک (HCl) | اسید قوی و موثر در حل کردن فلزات، اما اکسیدکننده نیست (ممکن است با فلزات گاز H₂ تولید کند). | کلریدهای فلزی تولید می کند؛ در صورت حرارت یا واکنش با اکسیدکننده ها گاز کلر یا بخارات HCl آزاد می کند. | برای تمیزکاری فلزات (مثلاً زدودن اکسید مس) و برخی مراحل بازیافت موثر است؛ پسماند اسیدی جامد برجای نمیگذارد. | یون های کلرید می توانند مشکل ساز باشند (برای تجهیزات خورنده اند و در صورت باقی ماندن به مواد باتری آسیب می زنند)؛ خطر گاز سمی Cl₂؛ مواد نیاز به شستشوی کامل برای حذف کلرید دارند. |
| اسیدهای آلی (مثلاً سیتریک) | اسیدهای آلی ضعیف؛ اکسیدکننده قوی نیستند (اغلب برای کمک به انحلال نیاز به H₂O₂ یا حرارت دارند). | کمپلکس های سیترات فلزی تولید می کنند؛ عموماً قابل تجزیه زیستی اما واکنش آنها کندتر است. | دوستدارتر محیط زیست؛ ملایم و انتخابی در حمله به مواد؛ بخارات کمخطرتر. | نرخ واکنش کندتر؛ ممکن است نتوانند همه اکسیدهای فلزی را کاملاً حل کنند؛ محلول های حاصل ممکن است نیاز به مراحل اضافی برای پردازش داشته باشند؛ در صورت حذف نشدن، بقایای آلی می توانند اختلال ایجاد کنند. |
| اسید فسفریک (H₃PO₄) | اسید با شدت متوسط، اکسیدکننده نیست؛ عمدتاً به عنوان منبع فسفات استفاده می شود. | فسفات های فلزی تولید می کند (که می توانند رسوب نامحلول باشند) و بخارات خطرناک ایجاد نمی کند. | در شیمی باتری های خاص استفاده می شود (مثلاً برای تأمین فسفات در کاتدهای LiFePO₄)؛ کار کردن با آن نسبتاً ایمن است. | برای حل کردن بسیاری از فلزات واسطه مناسب نیست؛ هرگونه پسماند فسفاتی باید مدیریت شود؛ در مقایسه با اسید نیتریک یا سولفوریک دامنه استفاده محدودی دارد. |
| اسید هیدروفلوئوریک (HF) | اسیدی بسیار واکنشپذیر (می تواند شیشه و بسیاری از اکسیدها را حل کند)؛ اکسیدکننده کلاسیک نیست ولی فوقالعاده مهاجم است. | فلوریدهای فلزی تولید می کند؛ بخارات بسیار سمی (بخار HF) و مایع خطرناک. | مفید برای حل کردن سیلیکا و برخی اکسیدهای پایدار (مثلاً در خالص سازی گرافیت همراه با HNO₃). | کار کردن با آن به شدت خطرناک است؛ نیاز به تجهیزات ویژه دارد؛ ضایعات فلوریدی خطرناک هستند؛ مگر در فرآیندهای خاص و در صورت ضرورت مطلق استفاده نمی شود. |
| اسیدهای مخلوط (مانند تیزاب سلطانی) | مخلوطی مانند HNO₃+HCl (تیزاب سلطانی) قدرت اکسیدکنندگی فوقالعاده بالایی دارد (فلزات نجیب را حل می کند). | نیترات ها و کلریدهای مختلط تولید می کند؛ حجم زیادی بخارات سمی آزاد می شود. | تقریباً هر چیزی را حل می کند (برای بازیابی فلزات گرانبها یا بقایای مقاوم استفاده می شود). | استفاده از آن برای تولید باتری بیش از حد شدید است؛ بسیار خورنده و خطرناک؛ به دلیل پیچیدگی مدیریت ضایعات معمولاً استفاده نمی شود. |
| بدون اسید (فرآیندهای بازی یا حرارتی) | برخی فرآیندها به جای اسید از محلول های بازی (مانند NaOH) یا عملیات دمای بالا استفاده می کنند. | ضایعات متفاوتی تولید می کند (مثلاً لجن یا سرباره در صورت ذوب) به جای نمک های اسیدی. | مشکلات کار با اسید را ندارد؛ به عنوان مثال، محلول بازی می تواند فویل آلومینیوم را حل کند یا ضایعات اسیدی را خنثی کند. | اغلب برای برخی وظایف کارایی کمتری دارد (مثلاً NaOH تنها آلومینیوم را حل می کند نه اکسیدهای کاتد)؛ روش های حرارتی انرژی بیشتری مصرف می کنند؛ ممکن است در مراحل بعدی برای تصفیه نهایی باز هم به اسید نیاز باشد. |
همان طور که جدول نشان می دهد اسید نیتریک واکنش پذیری بالای خود را با خروجی های تمیزتر پس از واکنش ترکیب کرده است (نیترات های محلولی که می توانند بازیافت شوند). در مقایسه با اسید سولفوریک ، استفاده از اسید نیتریک از تولید حجم زیادی پسماند جامد جلوگیری می کند. در مقایسه با HCl ، این اسید از آلودگی با کلرید جلوگیری می کند ، که امری حیاتی است زیرا حتی مقادیر جزئی کلرید می تواند به عملکرد باتری آسیب برساند. هرچند اسیدهای آلی و رویکردهای ملایم تر در کاربردهای خاص خود مفیدند اما هنوز نمی توانند از نظر کارایی با اسید نیتریک در وظایف اصلی تولید باتری رقابت کنند. هر اسیدی نقش خاص خود را دارد ، اما اسید نیتریک در صورت رعایت احتیاطات لازم ترکیبی متوازن از اثربخشی و ضایعات قابلکنترل را ارائه می دهد.
مزایای استفاده از اسید نیتریک در تولید باتری
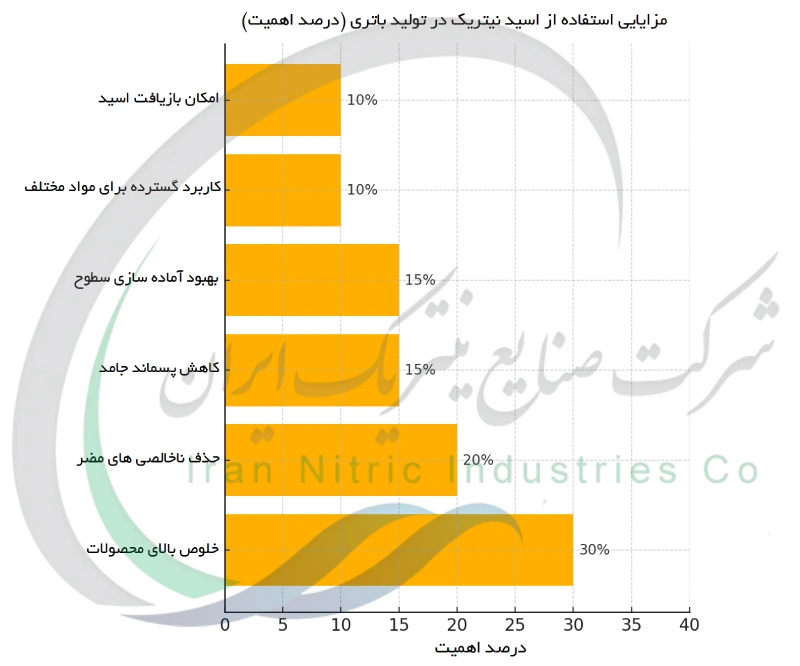
استفاده از اسید نیتریک در تولید باتری مزایای قابل توجهی دارد. مهم ترین آن دستیابی به خلوص بالای محصولات است ، زیرا واکنش های آن معمولاً نیترات های محلول در آب ایجاد می کند که جداسازی مواد را بدون باقی ماندن ناخالصی آسان می سازد. برخلاف فرآیندهای سولفاتی که ممکن است سولفات باقی بگذارند و به عملکرد باتری آسیب بزنند ، این روش تمیزتر است. قدرت اکسیدکنندگی بالای اسید نیتریک نیز به تجزیه مواد سرسخت و حذف باقی مانده های آلی کمک کرده و سطوح الکترود را برای پوشش دهی یا نفوذ بهتر الکترولیت آماده می کند. این ماده همه کاره است و برای تیمار فلزات ، کربن ها و دیگر مواد قابل استفاده است. همچنین امکان اجرای فرآیند حلقه بسته با بازیافت گازهای NOx و تبدیل دوباره آن ها به اسید نیتریک وجود دارد که علاوه بر بهبود بازده به کاهش ضایعات و هزینه های بلندمدت کمک می کند.
اقدامات ایمنی برای کار با اسید نیتریک
کار با اسید نیتریک به علت خاصیت خورندگی و سمیت بالا نیازمند رعایت دقیق اصول ایمنی است. کارکنان باید آموزش کامل در زمینه کار با اسید و اقدامات اضطراری ببینند. استفاده از تجهیزات حفاظت شخصی مانند دستکش مقاوم ، شیلد صورت ، عینک ایمنی و پیش بند ضروری است، زیرا حتی تماس جزئی می تواند باعث سوختگی شدید یا کوری شود. تهویه مناسب برای جلوگیری از تجمع گاز سمی NO₂ حیاتی است و استفاده از هود بخار در فرآیندهای باز توصیه می شود. این اسید باید در ظروف مقاوم و محفظه ثانویه ذخیره شود و دور از مواد آلی یا قابل اشتعال قرار گیرد. همچنین وجود کیت خنثی سازی حاوی مواد قلیایی مانند بی کربنات سدیم ضروری است. با رعایت این موارد می توان از اسید نیتریک در صنعت باتری به طور ایمن و مؤثر استفاده کرد.
نوآوری ها و پژوهش های جدید درباره اسید نیتریک در باتری ها
پژوهش های اخیر نشان می دهد که اسید نیتریک نقش مهمی در نوآوری های حوزه تولید و بازیافت باتری دارد. فرآیندهای نوینی برای ساخت پیش ماده های کاتد از محلول های غلیظ نیترات استفاده می کنند که تمامی محصولات جانبی را بازیافت کرده و ضایعات را به طور چشمگیری کاهش می دهند. در برخی واحدهای آزمایشی تقریباً تمام اسید نیتریک در چرخه تولید بازیابی و مجدداً استفاده می شود که نشان دهنده امکان تولید سبزتر است. در حوزه باتری های نسل بعدی ایده باتری روی-نیترات مطرح شده که علاوه بر ذخیره انرژی ، آلاینده های نیتراتی فاضلاب را به ترکیبات مفید تبدیل می کند. همچنین استفاده مستقیم از اسید نیتریک یا مشتقات آن در طرح هایی مانند باتری اسید نیتریک برای افزایش طول عمر و حذف فلزات سنگین در حال بررسی است. ترکیب تیمار اسید نیتریک با فناوری هایی چون پلاسما و بهینه سازی فرآیند لیچینگ نیز موجب بهبود کیفیت مواد الکترود و افزایش کارایی بازیافت با مصرف کمتر اسید می شود.




