فهرست عناوین
- اهمیت خالص سازی اسید نیتریک در آزمایشگاه
- ناخالصی های رایج در اسید نیتریک صنعتی
- روش های کلی برای خالص سازی اسید نیتریک
- تقطیر ساده : اولین گام در خالص سازی اسید نیتریک
- تقطیر آزئوتروپیک اسید نیتریک : چگونه خلوص بالاتر به دست آوریم ؟
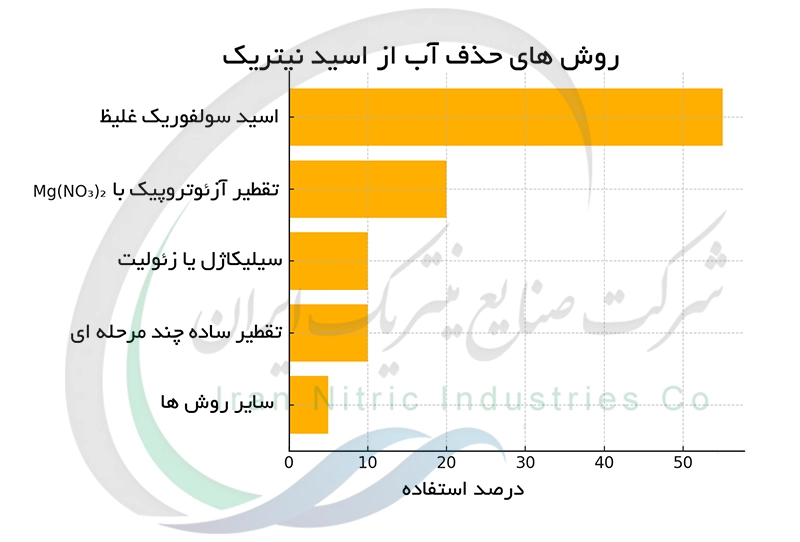
- استفاده از اسید سولفوریک برای حذف آب از اسید نیتریک
- روش تصفیه اسید نیتریک با استفاده از کربن فعال
- تکنیک های سردسازی و کریستالیزاسیون برای خالص سازی اسید نیتریک
- استفاده از روش های تبادل یونی برای حذف یون های مزاحم از اسید نیتریک
- نقش گازدهی و حباب دهی در خالص سازی اسید نیتریک
- بررسی روش های حذف اکسیدهای نیتروژن از اسید نیتریک
- چگونه می توان اسید نیتریک فوق خالص (Ultra Pure) تهیه کرد ؟
- کاربردهای اسید نیتریک خالص در صنایع و تحقیقات علمی
نوشته شده توسط شرکت صنایع نیتریک ایران
منتشر شده توسط شرکت صنایع نیتریک ایران
تاریخ انتشار مقاله : 21-01-1404
تاریخ بروزرسانی مقاله : 21-01-1404
تعداد کلمات : 1500
آدرس مقاله : لینک مقاله
روش های خالص سازی اسید نیتریک در آزمایشگاه

اهمیت خالص سازی اسید نیتریک در آزمایشگاه
اسید نیتریک صنعتی حاوی ناخالصی هایی است که بر دقت و قابلیت اطمینان آزمایش ها اثر می گذارند. این ناخالصی ها در واکنش ها اختلال ایجاد کرده ، نتایج را مغشوش می کنند و حتی به تجهیزات آزمایشگاهی آسیب می رسانند. خلوص بالا به ویژه در تحقیقات دقیق ، سنتز ترکیبات خاص و تجزیه و تحلیل های حساس شیمیایی ضروری است. از طرفی واکنش پذیری و کارایی اسید نیتریک در کاربردهای تخصصی به میزان خلوص آن بستگی دارد. بنابراین خالص سازی برای دستیابی به نتایج قابل اعتماد و دقیق در کنار بررسی مواد اولیه مورد نیاز برای تولید آزمایشگاهی اسید نیتریک ، پیش نیاز است.
ناخالصی های رایج در اسید نیتریک صنعتی
اسید نیتریک صنعتی اغلب حاوی ناخالصی هایی است که کیفیت آن را پایین می آورند و در کاربردهای حساس آزمایشگاهی مشکل ایجاد می کنند. آب یکی از رایج ترین ناخالصی هاست که رطوبت را افزایش می دهد و بر غلظت اسید اثر می گذارد. اکسیدهای نیتروژن مانند N₂O₄ و NO₂ نیز به طور معمول وجود دارند که واکنش ها را مختل می کنند. فلزات سنگین مانند آهن ، مس و نیکل به عنوان ناخالصی های جزئی وجود دارند و در برخی آزمایش ها باعث خطا می شوند. وجود این ناخالصی ها می تواند بر دقت اندازه گیری ها و کیفیت نتایج تأثیر بگذارد و حتی در برخی موارد واکنش های جانبی ناخواسته ایجاد کنند.
| ردیف | نام ناخالصی | فرمول شیمیایی | منبع ورود به اسید نیتریک | تأثیر بر کیفیت | روش حذف یا کنترل |
|---|---|---|---|---|---|
| 1 | آب | H₂O | باقیمانده از فرآیند تولید یا ذخیرهسازی | کاهش خلوص، تأثیر در واکنشها | تقطیر یا خشکسازی |
| 2 | دیاکسید نیتروژن | NO₂ | تولید در فرآیند اکسیداسیون آمونیاک | رنگ قهوهای، افزایش خورندگی | تقطیر مجدد با خنکسازی مناسب |
| 3 | نیتریک اسید رقیق | HNO₃ (غلظت پایین) | اختلاط با اسید بازیافتی | کاهش قدرت اسیدی | تغلیظ مجدد |
| 4 | نیتراتهای فلزی | مانند Fe(NO₃)₃ | آلودگی از تجهیزات فلزی | کدر شدن، ایجاد رسوب | فیلتراسیون و استفاده از ظروف مقاوم |
| 5 | ترکیبات آلی | CH₃COOH، C₆H₆ و ... | ورود از مواد اولیه آلوده | ناپایداری حرارتی، واکنشپذیری زیاد | تقطیر دقیق یا اکسیداسیون |
| 6 | آمونیاک | NH₃ | باقیمانده از واکنشهای ناقص | تغییر pH، کاهش خاصیت اسیدی | کنترل شرایط واکنش و تصفیه گازها |
روش های کلی برای خالص سازی اسید نیتریک
خالص سازی اسید نیتریک در آزمایشگاه با هدف افزایش خلوص آن انجام می شود. روش های متفاوتی برای این منظور وجود دارد. تقطیر روشی معمول برای حذف ناخالصی های فرار و آب است. تبخیر جزئی نیز برای جداسازی اجزا با نقاط جوش متفاوت کاربرد دارد. حذف آب با استفاده از مواد خشک کننده مانند اسید سولفوریک غلیظ باعث افزایش غلظت اسید می شود. همچنین از جاذب های انتخابی برای حذف ناخالصی های خاص استفاده می شود. روش مناسب به نوع و مقدار ناخالصی ها بستگی دارد.
تقطیر ساده : اولین گام در خالص سازی اسید نیتریک
تقطیر راهکاری مؤثر برای افزایش خلوص اسید نیتریک است. این روش بر پایه تفاوت در نقاط جوش اجزای مخلوط عمل می کند. بخار اسید نیتریک با دمای جوش پایین تر زودتر تبخیر شده و در کندانسور خنک و جمع آوری می شود. این روش ناخالصی های فرّار و آب اضافی را به طور مؤثری حذف می کند. با این حال برای جداسازی کامل از سایر ناخالصی ها کافی نیست و ممکن است به روش های تکمیلی نیاز باشد. راندمان تقطیر به عوامل مختلفی از جمله سرعت حرارت دهی و طراحی دستگاه تقطیر بستگی دارد.
تقطیر آزئوتروپیک اسید نیتریک : چگونه خلوص بالاتر به دست آوریم ؟
اسید نیتریک 68% با آب آزئوتروپ تشکیل می دهد یعنی نمی توان آن را با تقطیر ساده به طور کامل از آب جدا کرد. برای غلظت بیشتر و افزایش خلوص از مواد جاذب رطوبت مانند اسید سولفوریک غلیظ استفاده می شود. این مواد آب را جذب کرده و اسید نیتریک تغلیظ شده باقی می ماند. سپس این اسید تغلیظ شده تقطیر می شود تا خلوص بالاتری حاصل شود. این روش مناسب برای حصول اسید نیتریک با خلوص بسیار بالا می باشد که برای اسید نیتریک استخراج طلا هم مورد استفاده قرار می گیرد. توجه به دقت در مرحله آب گیری برای رسیدن به بهترین نتیجه مهم است.
استفاده از اسید سولفوریک برای حذف آب از اسید نیتریک
اسید سولفوریک به دلیل میل ترکیبی بسیار زیادش با آب عامل مؤثری برای خشک کردن اسید نیتریک است. در این روش اسید نیتریک با اسید سولفوریک غلیظ مخلوط می شود. اسید سولفوریک آب موجود در اسید نیتریک را جذب می کند و غلظت اسید نیتریک افزایش می یابد. این روش معمولاً به عنوان مرحله ای قبل از تقطیر برای افزایش راندمان جداسازی استفاده می شود. انتخاب غلظت اسید سولفوریک و زمان تماس نقش مهمی در میزان آبگیری دارد. پس از جداسازی ، اسید نیتریک غلیظ تر به دست می آید.
روش تصفیه اسید نیتریک با استفاده از کربن فعال
کربن فعال به دلیل سطح ویژه بالای خود جاذب مؤثری برای انواع ناخالصی هاست. در خالص سازی اسید نیتریک ، کربن فعال ترکیبات آلی و رنگدانه های محلول را جذب می کند. اسید نیتریک از ستون حاوی کربن فعال عبور داده می شود. مولکول های آلی و ناخالصی های رنگی به سطح کربن فعال می چسبند و اسید نیتریک تصفیه شده از ستون خارج می شود. میزان جذب به عوامل مختلفی مانند نوع کربن فعال ، اندازه ذرات ، غلظت ناخالصی ها و زمان تماس بستگی دارد. پس از استفاده کربن فعال اشباع شده باید تعویض شود یا احیا گردد. این روش در بهبود شفافیت و خلوص اسید نیتریک مؤثر است.
تکنیک های سردسازی و کریستالیزاسیون برای خالص سازی اسید نیتریک
کاهش دما (سردسازی) اسید نیتریک باعث کاهش حلالیت برخی ناخالصی ها می شود. این ناخالصی ها به صورت رسوب از محلول جدا می شوند. با این روش ناخالصی های جامد و نامحلول در دمای پایین رسوب کرده و به راحتی از اسید جدا می شوند. به عنوان مثال برخی نمک های فلزی می توانند با سرد کردن اسید نیتریک رسوب کنند. کریستالیزاسیون فرآیندی است که در آن خالص ترین بخش اسید نیتریک با کاهش دما به صورت بلور جدا می شود. این روش برای جداسازی ناخالصی های محلول که در دمای پایین حلالیت کمتری دارند ، کاربرد دارد. بازده این روش به عوامل مختلفی مانند سرعت سرد کردن و غلظت اولیه اسید بستگی دارد. بعد از جداسازی رسوب یا بلورها ، اسید نیتریک با خلوص بالاتر به دست می آید.
استفاده از روش های تبادل یونی برای حذف یون های مزاحم از اسید نیتریک
تبادل یونی روشی موثر برای تصفیه اسید نیتریک از یون های ناخواسته است. رزین های تبادل یونی مواد جامدی با ساختار متخلخل هستند که یون های فلزی و دیگر ناخالصی های محلول را جذب می کنند. اسید نیتریک از ستونی حاوی رزین عبور داده می شود. یون های مزاحم به رزین می چسبند و اسید تصفیه شده از ستون خارج می شود. نوع رزین و شرایط عملیاتی مانند PH و دما تاثیر قابل توجهی بر میزان حذف یون ها دارد. پس از اشباع رزین نیاز به احیا یا تعویض دارد. این روش برای حذف یون های فلزی سنگین ، کاتیون ها و آنیون های موجود در اسید نیتریک مناسب است.
نقش گازدهی و حباب دهی در خالص سازی اسید نیتریک
حباب دهی گاز خالص راهی برای زدودن گازهای محلول ناخواسته در اسید نیتریک است. عبور گازهایی مانند نیتروژن یا هوا از اسید باعث می شود گازهای محلول مانند دی اکسید نیتروژن (NO2) از محلول خارج شوند. این عمل با ایجاد حباب های گاز در اسید ، افزایش سطح تماس گاز و مایع و انتشار گازهای محلول به فاز گاز انجام می شود. بهینه سازی این فرآیند شامل کنترل دبی گاز دمای اسید و زمان تماس است. استفاده از گاز خنثی مانند نیتروژن جلوگیری از اکسیداسیون و تغییرات در ترکیب اسید را تضمین می کند. حباب دهی به ویژه برای حذف گازهای فرار و افزایش خلوص اسید نیتریک مفید است.
بررسی روش های حذف اکسیدهای نیتروژن از اسید نیتریک
اکسیدهای نیتروژن مانند NO و NO₂ ناخالصی های رایج در اسید نیتریک هستند که رنگ زرد یا قرمز به آن می دهند. حذف این اکسیدها برای دستیابی به اسید با خلوص بالا حیاتی است. روش های مختلفی برای این منظور وجود دارد. تقطیر یکی از روش های مؤثر است. با تقطیر اکسیدهای نیتروژن فرار قبل از اسید نیتریک تبخیر شده و جدا می شوند. همچنین می توان از اکسید کننده هایی مانند پراکسید هیدروژن استفاده کرد. اکسید کننده ها اکسیدهای نیتروژن را به نیترات تبدیل می کنند که در اسید نیتریک محلول نیستند و می توان آن ها را به راحتی از محلول جدا کرد. انتخاب روش مناسب به غلظت اکسیدهای نیتروژن و سایر ناخالصی های موجود بستگی دارد. در برخی موارد ترکیبی از روش ها برای رسیدن به حداکثر خلوص لازم است.
چگونه می توان اسید نیتریک فوق خالص (Ultra Pure) تهیه کرد ؟
تهیه اسید نیتریک فوق خالص نیازمند روش های پیشرفته تصفیه است. تقطیر در خلا روشی مؤثر برای حذف ناخالصی های فرار است. کاهش فشار در تقطیر نقطه جوش اسید نیتریک را پایین می آورد و از تجزیه آن در دماهای بالا جلوگیری می کند. استفاده از جاذب های تخصصی مانند رزین های تبادل یونی با انتخاب پذیری بالا برای حذف یون های فلزی و ناخالصی های یونی ضروری است. روش های پیشرفته تبخیر مانند تبخیر در جریان گاز بی اثر باعث حذف آب و سایر ناخالصی های فرار می شود. به علاوه برای رسیدن به بالاترین خلوص از فیلتراسیون با فیلترهای با دقت بسیار بالا استفاده می شود. کنترل دقیق پارامترهای عملیاتی مانند دما و فشار برای کسب بهترین نتیجه ضروری است.
کاربردهای اسید نیتریک خالص در صنایع و تحقیقات علمی
در صنایع الکترونیک برای تولید مدارهای مجتمع و تراشه های نیمه هادی استفاده می شود. در ساخت مواد منفجره نیز مورد نیاز است. همچنین در تولید رنگ ها ، داروها و دیگر مواد شیمیایی مهم کاربرد دارد. در آزمایشگاه ها اسید نیتریک با خلوص بالا برای آنالیزهای شیمیایی دقیق ، تهیه محلول های استاندارد و مطالعات پژوهشی استفاده می شود. خلوص بالا نتایج دقیق تر و قابل اعتمادتری را در مطالعات تحقیقاتی فراهم می کند. کاربردهای اسید نیتریک با خلوص بالا پیوسته در حال افزایش است.




